你能想象么?每个宝宝在出生前,都曾是一位在“饥饿”边缘疯狂赶工的建筑大师。由于妈妈的营养需经胎盘输送给宝宝,宝宝的血糖浓度天然低于妈妈,这构成了一种“生理性低糖”的环境。对成年肝脏而言,低糖本是停工节能的指令,但在宝宝肝脏里,却是一场锁定生长特权的逆袭。
2026年3月13日,浙江大学医学院黄荷凤院士团队联合厦门大学生命科学学院林圣彩院士团队,在《Vita》上在线发表了《TRPV4 acetylation in prenatal liver prevents low glucose-induced inhibition of mTORC1 and safeguards fetal development》研究成果,揭开了这把守护生命初期健康的“分子钥匙”。这也是《Vita》新版官网首篇上线的原创研究论文。
宝宝为什么不怕低血糖?
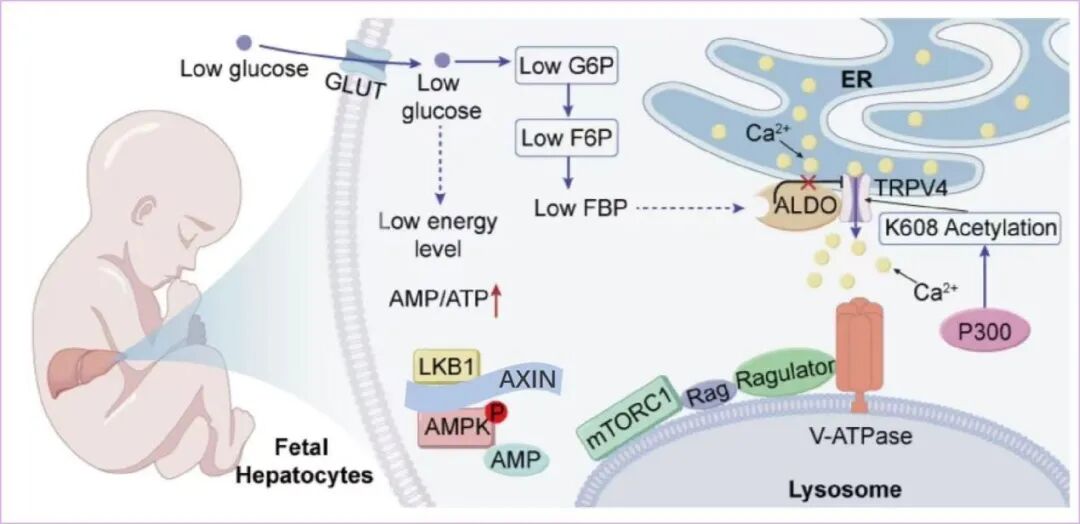
为了让营养顺畅流入,胎盘会主动将一部分葡萄糖截留消耗,导致宝宝血糖天然低于妈妈。这在成年细胞逻辑里是“饥饿”的铁证。一旦血糖降低,细胞内的能量监测员AMPK会立刻警报,关停负责建设的指挥官mTORC1。
然而,研究团队在宝宝肝脏中发现了一个神奇的现象:即便在低糖时监测员已报警,指挥官mTORC1依然稳如泰山,指挥着蛋白质全速合成。这种“预警不误建设”的独特状态,保障了宝宝在降生前完成最高效的组织基建。
更有趣的是,这种“代谢豁免权”极其罕见且短暂。研究发现,无论是实验室常用的模式细胞(如HEK293T和MEF),还是成年小鼠的肝脏细胞,都无法获得这种特权。它似乎是专为胎儿期定制的“限时福利”——一旦宝宝出生超过24小时,这种能力便会瞬间消失,肝脏会准时切换回成年人的饥饿感应模式。
是谁为感应窗口按下了常开键?
既然警报已经在响,宝宝肝脏是怎么做到“充耳不闻”的?答案就藏在一个名为TRPV4的信号窗口里。
在成年人的肝脏中,这个窗口对低糖极其敏感:一旦感知到糖分暴跌,便会迅速关闭,从而引发下游的一系列停工反应。但在宝宝肝脏里,这个窗口却像被按下了“常开键”。科学家发现,胎儿肝脏中活跃着一种名为p300的酶,它像个精密的“检修工”,在TRPV4蛋白的K608位点贴上了一枚名为“乙酰化”的化学标签。这枚标签就像一个微型的信号屏蔽器,将TRPV4通道固定在开启状态。只要这扇窗户不关,低糖带来的饥饿信号就无法传达到指挥部,总指挥mTORC1便能无视环境贫瘠,心无旁骛地指挥蛋白质全速生产。
为了验证这层“屏蔽罩”的重要性,研究团队培育了TRPV4-K608R位点突变的转基因胎鼠——相当于把这个“常开键”人为关闭。结果令人震撼:失去了这层保护,胎鼠肝脏发育迅速停滞,部分个体甚至无法存活。这证明了TRPV4 K608位的乙酰化修饰,正是保障宝宝在逆境中顽强成长的生命防线。
这种早期生长策略会影响未来健康吗?
这种生命早期的自适应逻辑,保障了胎儿在资源受限时的发育,然而,却也在细胞层面留下了长久的代谢编程印记。从全生命周期健康的视角来看,这种早期设定的分子程序,既是生命初期的生存保障,也可能成为影响成年健康的原始参数。
这意味着,如果生命早期的宫内环境遭遇剧烈波动——例如母体代谢紊乱导致血糖水平异常,这套原本为了应对低糖环境而演化的保护机制就可能由于与环境不匹配而发生失衡。这种分子层面的早期印记具有跨越数十年的影响力,可能增加成年期患上肥胖、糖尿病等代谢疾病的风险。
读懂这段发育机制,不仅是在解析前沿科学,更是为了让我们从源头上审视全生命周期健康,为一生的福祉打下更坚实的认知基础。
该研究由浙江大学医学院黄荷凤院士、厦门大学生命科学学院林圣彩院士、复旦大学附属妇产科医院丁国莲教授、厦门大学生命科学学院张宸崧教授担任共同通讯作者。浙江大学医学院附属第四医院张辰颉医师、复旦大学附属妇产科医院余传金助理研究员为共同第一作者。研究得到了国家自然科学基金、国家重点研发计划等项目的资助。
内容来源:医学院
今日编辑:浙江大学融媒体中心学生记者团 周徵玥
责任编辑:王欢 董晓萌